FDA разрабатывает нормативную базу для медицинских устройств, связанных с искусственным интеллектом
|
By HospiMedica International staff writers Posted on 08 Aug 2019 |
Управление США по контролю качества пищевых продуктов и лекарственных средств (US Food and Drug Administration - FDA; Силвер-Спринг, штат Мэриленд, США) рассматривает новую нормативно-правовую базу, специально разработанную для содействия разработке безопасных и эффективных медицинских устройств, использующих современные алгоритмы искусственного интеллекта (ИИ).
Алгоритмы ИИ уже используются, чтобы помочь в скрининге заболеваний и предоставлении рекомендаций по лечению. До настоящего времени FDA выдавало регистрационное удостоверение и разрешение на продажу на технологии ИИ, также называемые "фиксированными" алгоритмами, которые не способны постоянно адаптироваться или обучаться при каждом использовании алгоритма. Производители модифицируют эти фиксированные алгоритмы в процессе обучения алгоритма с использованием новых данных, с последующей ручной проверкой и валидацией обновленного алгоритма. В случае традиционного программного обеспечения в качестве медицинского устройства спонсор должен предоставить документ, демонстрирующий безопасность и эффективность модификаций.
Однако алгоритмы машинного обучения, которые постоянно развиваются и называются адаптивными, или непрерывно обучающимися алгоритмами, не требуют ручной модификации для включения обучения или обновлений, поскольку они могут учиться на основе новых пользовательских данных, представленных им в реальных условиях применения. Например, алгоритм, который обнаруживает образования рака молочной железы на маммограммах, может научиться повышать достоверность, с которой он идентифицирует поражения как раковые, или идентифицировать конкретные подтипы рака молочной железы, постоянно обучаясь на основе реального использования и обратной связи.
В настоящее время FDA изучает структуру, которая позволила бы вносить изменения в алгоритмы из реального обучения и адаптации, одновременно обеспечивая безопасность и эффективность программного обеспечения как медицинского устройства. FDA рассматривает вопрос о том, как подход, позволяющий оценивать и контролировать программный продукт от его предрыночной разработки до производительности после выхода на рынок, может обеспечить разумную гарантию безопасности и эффективности и позволить регулирующим агентствам принять итеративный характер этих ИИ-продуктов, обеспечивая при этом соблюдение стандартов безопасности и эффективности.
"Мы делаем первый шаг к разработке нового, индивидуального подхода, чтобы помочь разработчикам вывести устройства искусственного интеллекта на рынок, выпустив документ для обсуждения. Другие шаги в будущем будут включать выпуск проекта руководства, которое будет основано на информации, которую мы получим. Наш подход будет сосредоточен на постоянно меняющейся природе этих перспективных технологий. Мы планируем использовать данные нам полномочия новыми способами, чтобы идти в ногу с быстрыми темпами инноваций и обеспечить безопасность этих устройств", — заявила FDA в своем пресс-релизе.
Ссылки по теме:
Управление США по контролю качества пищевых продуктов и лекарственных средств
Алгоритмы ИИ уже используются, чтобы помочь в скрининге заболеваний и предоставлении рекомендаций по лечению. До настоящего времени FDA выдавало регистрационное удостоверение и разрешение на продажу на технологии ИИ, также называемые "фиксированными" алгоритмами, которые не способны постоянно адаптироваться или обучаться при каждом использовании алгоритма. Производители модифицируют эти фиксированные алгоритмы в процессе обучения алгоритма с использованием новых данных, с последующей ручной проверкой и валидацией обновленного алгоритма. В случае традиционного программного обеспечения в качестве медицинского устройства спонсор должен предоставить документ, демонстрирующий безопасность и эффективность модификаций.
Однако алгоритмы машинного обучения, которые постоянно развиваются и называются адаптивными, или непрерывно обучающимися алгоритмами, не требуют ручной модификации для включения обучения или обновлений, поскольку они могут учиться на основе новых пользовательских данных, представленных им в реальных условиях применения. Например, алгоритм, который обнаруживает образования рака молочной железы на маммограммах, может научиться повышать достоверность, с которой он идентифицирует поражения как раковые, или идентифицировать конкретные подтипы рака молочной железы, постоянно обучаясь на основе реального использования и обратной связи.
В настоящее время FDA изучает структуру, которая позволила бы вносить изменения в алгоритмы из реального обучения и адаптации, одновременно обеспечивая безопасность и эффективность программного обеспечения как медицинского устройства. FDA рассматривает вопрос о том, как подход, позволяющий оценивать и контролировать программный продукт от его предрыночной разработки до производительности после выхода на рынок, может обеспечить разумную гарантию безопасности и эффективности и позволить регулирующим агентствам принять итеративный характер этих ИИ-продуктов, обеспечивая при этом соблюдение стандартов безопасности и эффективности.
"Мы делаем первый шаг к разработке нового, индивидуального подхода, чтобы помочь разработчикам вывести устройства искусственного интеллекта на рынок, выпустив документ для обсуждения. Другие шаги в будущем будут включать выпуск проекта руководства, которое будет основано на информации, которую мы получим. Наш подход будет сосредоточен на постоянно меняющейся природе этих перспективных технологий. Мы планируем использовать данные нам полномочия новыми способами, чтобы идти в ногу с быстрыми темпами инноваций и обеспечить безопасность этих устройств", — заявила FDA в своем пресс-релизе.
Ссылки по теме:
Управление США по контролю качества пищевых продуктов и лекарственных средств
Latest Бизнес News
Channels
Artificial Intelligence
view channel
AI-Powered Algorithm to Revolutionize Detection of Atrial Fibrillation
Atrial fibrillation (AFib), a condition characterized by an irregular and often rapid heart rate, is linked to increased risks of stroke and heart failure. This is because the irregular heartbeat in AFib... Read more
AI Diagnostic Tool Accurately Detects Valvular Disorders Often Missed by Doctors
Doctors generally use stethoscopes to listen for the characteristic lub-dub sounds made by heart valves opening and closing. They also listen for less prominent sounds that indicate problems with these valves.... Read moreCritical Care
view channel
Wheeze-Counting Wearable Device Monitors Patient's Breathing In Real Time
Lung diseases like asthma, chronic obstructive pulmonary disease (COPD), lung cancer, bronchitis, and infections such as pneumonia, rank among the leading causes of death worldwide. Traditionally, medical... Read more
Wearable Multiplex Biosensors Could Revolutionize COPD Management
Chronic obstructive pulmonary disease (COPD) ranks as the third leading cause of death worldwide. Acute exacerbations of COPD (AECOPD), which are often triggered by lung infections, accelerate the disease's... Read moreSurgical Techniques
view channel
Flexible Microdisplay Visualizes Brain Activity in Real-Time To Guide Neurosurgeons
During brain surgery, neurosurgeons need to identify and preserve regions responsible for critical functions while removing harmful tissue. Traditionally, neurosurgeons rely on a team of electrophysiologists,... Read more.jpg)
Next-Gen Computer Assisted Vacuum Thrombectomy Technology Rapidly Removes Blood Clots
Pulmonary embolism (PE) occurs when a blood clot blocks one of the arteries in the lungs. Often, these clots originate from the leg or another part of the body, a condition known as deep vein thrombosis,... Read more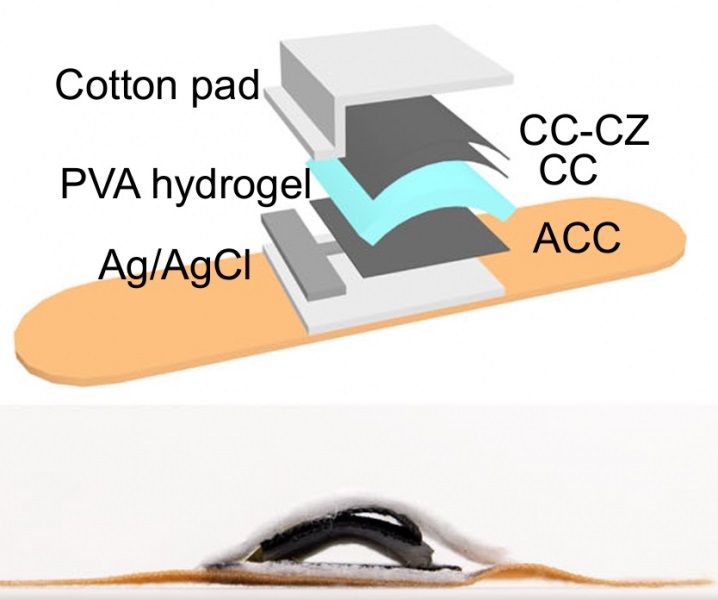
Hydrogel-Based Miniaturized Electric Generators to Power Biomedical Devices
The development of engineered devices that can harvest and convert the mechanical motion of the human body into electricity is essential for powering bioelectronic devices. This mechanoelectrical energy... Read moreWearable Technology Monitors and Analyzes Surgeons' Posture during Long Surgical Procedures
The physical strain associated with the static postures maintained by neurosurgeons during long operations can lead to fatigue and musculoskeletal problems. An objective assessment of surgical ergonomics... Read morePatient Care
view channel
Surgical Capacity Optimization Solution Helps Hospitals Boost OR Utilization
An innovative solution has the capability to transform surgical capacity utilization by targeting the root cause of surgical block time inefficiencies. Fujitsu Limited’s (Tokyo, Japan) Surgical Capacity... Read more
Game-Changing Innovation in Surgical Instrument Sterilization Significantly Improves OR Throughput
A groundbreaking innovation enables hospitals to significantly improve instrument processing time and throughput in operating rooms (ORs) and sterile processing departments. Turbett Surgical, Inc.... Read more
Next Gen ICU Bed to Help Address Complex Critical Care Needs
As the critical care environment becomes increasingly demanding and complex due to evolving hospital needs, there is a pressing requirement for innovations that can facilitate patient recovery.... Read moreGroundbreaking AI-Powered UV-C Disinfection Technology Redefines Infection Control Landscape
Healthcare-associated infection (HCAI) is a widespread complication in healthcare management, posing a significant health risk due to its potential to increase patient morbidity and mortality, prolong... Read moreHealth IT
view channel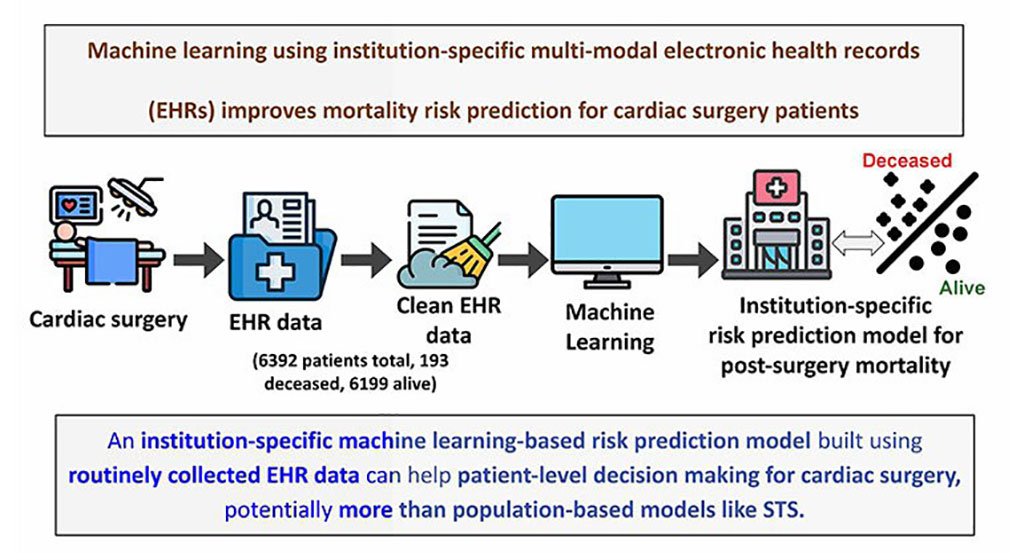
Machine Learning Model Improves Mortality Risk Prediction for Cardiac Surgery Patients
Machine learning algorithms have been deployed to create predictive models in various medical fields, with some demonstrating improved outcomes compared to their standard-of-care counterparts.... Read more
Strategic Collaboration to Develop and Integrate Generative AI into Healthcare
Top industry experts have underscored the immediate requirement for healthcare systems and hospitals to respond to severe cost and margin pressures. Close to half of U.S. hospitals ended 2022 in the red... Read more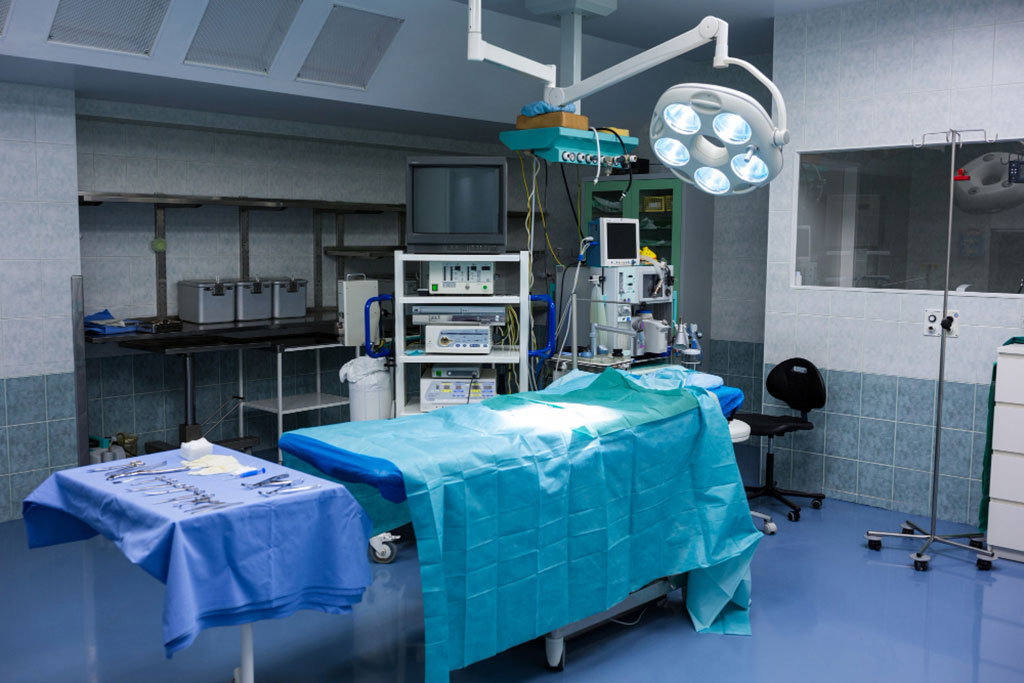
AI-Enabled Operating Rooms Solution Helps Hospitals Maximize Utilization and Unlock Capacity
For healthcare organizations, optimizing operating room (OR) utilization during prime time hours is a complex challenge. Surgeons and clinics face difficulties in finding available slots for booking cases,... Read more
AI Predicts Pancreatic Cancer Three Years before Diagnosis from Patients’ Medical Records
Screening for common cancers like breast, cervix, and prostate cancer relies on relatively simple and highly effective techniques, such as mammograms, Pap smears, and blood tests. These methods have revolutionized... Read morePoint of Care
view channel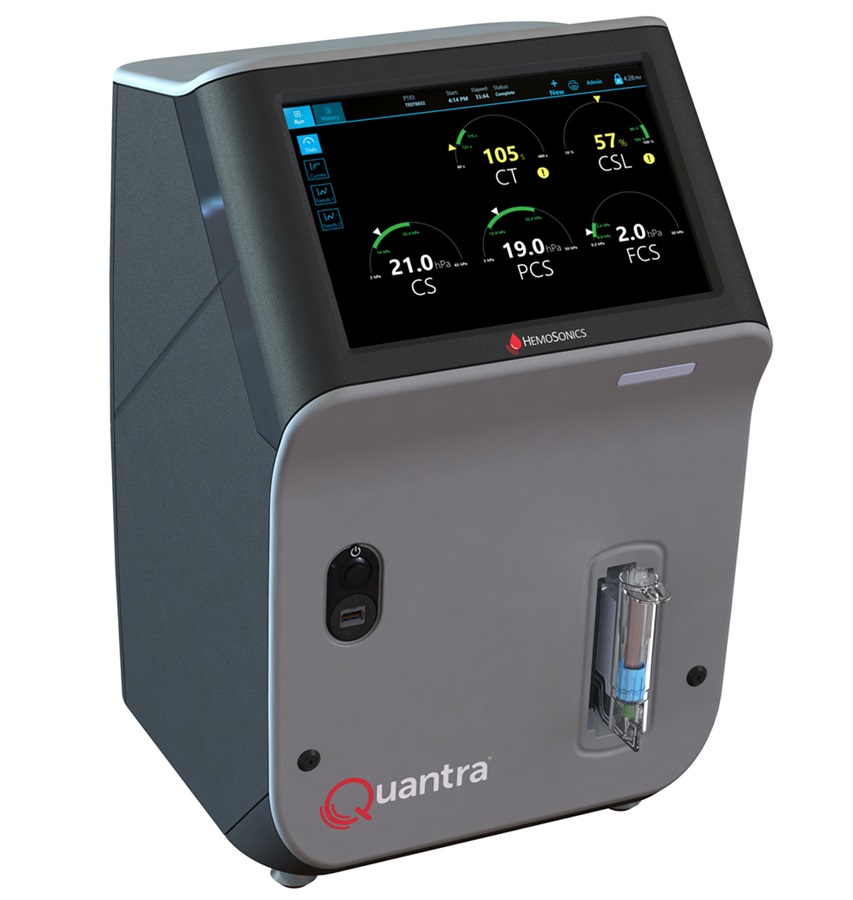
Critical Bleeding Management System to Help Hospitals Further Standardize Viscoelastic Testing
Surgical procedures are often accompanied by significant blood loss and the subsequent high likelihood of the need for allogeneic blood transfusions. These transfusions, while critical, are linked to various... Read more
Point of Care HIV Test Enables Early Infection Diagnosis for Infants
Early diagnosis and initiation of treatment are crucial for the survival of infants infected with HIV (human immunodeficiency virus). Without treatment, approximately 50% of infants who acquire HIV during... Read more
Whole Blood Rapid Test Aids Assessment of Concussion at Patient's Bedside
In the United States annually, approximately five million individuals seek emergency department care for traumatic brain injuries (TBIs), yet over half of those suspecting a concussion may never get it checked.... Read more
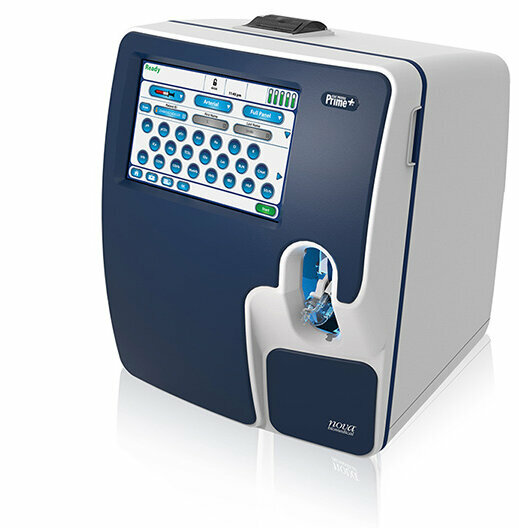
New Generation Glucose Hospital Meter System Ensures Accurate, Interference-Free and Safe Use
A new generation glucose hospital meter system now comes with several features that make hospital glucose testing easier and more secure while continuing to offer accuracy, freedom from interference, and... Read moreBusiness
view channel
Johnson & Johnson Acquires Cardiovascular Medical Device Company Shockwave Medical
Johnson & Johnson (New Brunswick, N.J., USA) and Shockwave Medical (Santa Clara, CA, USA) have entered into a definitive agreement under which Johnson & Johnson will acquire all of Shockwave’s... Read more











.jpg)
